2021年10月12日,中国科学院武汉病毒研究所/病毒学国家重点实验室周溪团队与复旦大学医学分子病毒学教育部/卫健委重点实验室陆路团队合作发表于《Immunity》杂志题为“Inhibition of viral suppressor of RNAi proteins by designerpeptides protects from enteroviral infection in vivo”的研究论文,首次揭示通过合理设计多肽类抑制剂,使其特异性靶向肠道病毒RNAi抑制子,能有效打破病毒VSR对RNAi的抑制,充分释放RNAi的抗病毒免疫功能,成为RNAi免疫机制在哺乳动物中依然存在的有力证明。由于该免疫机制在细胞与动物体内水平展现出的良好抗病毒活性,以及较高的安全性,使其临床开发的潜力极高。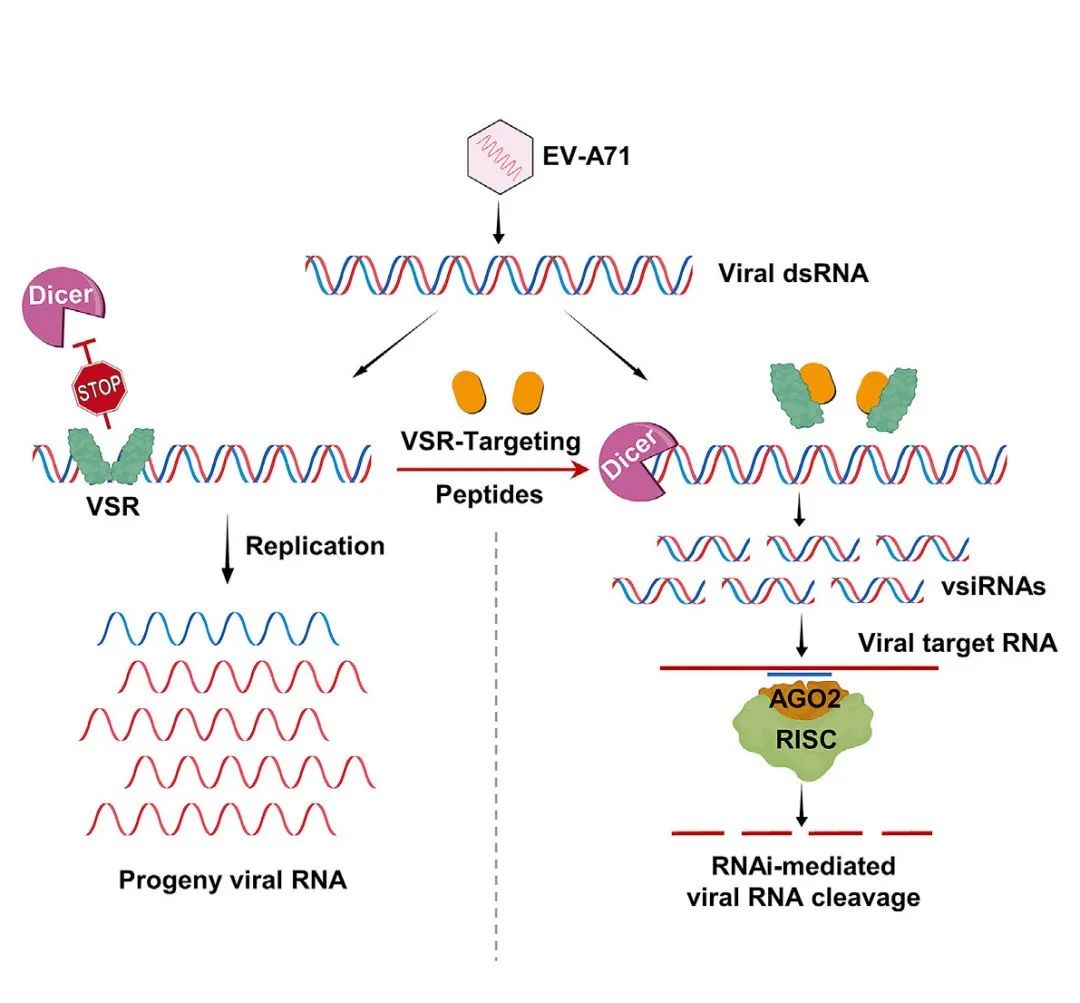
免疫战争:随时参战的双方,手段频出的战场
从宏观尺度的刺、角、爪、牙,到细胞层面的吞噬、溶解、毒杀,再到分子结构的切割、干扰、降解;从体外到体内、细胞外到细胞内:欢迎来到既分高下,也决生死的战场——一场随时打响的免疫战争。

RNAi——天然高效的抗病毒免疫机制
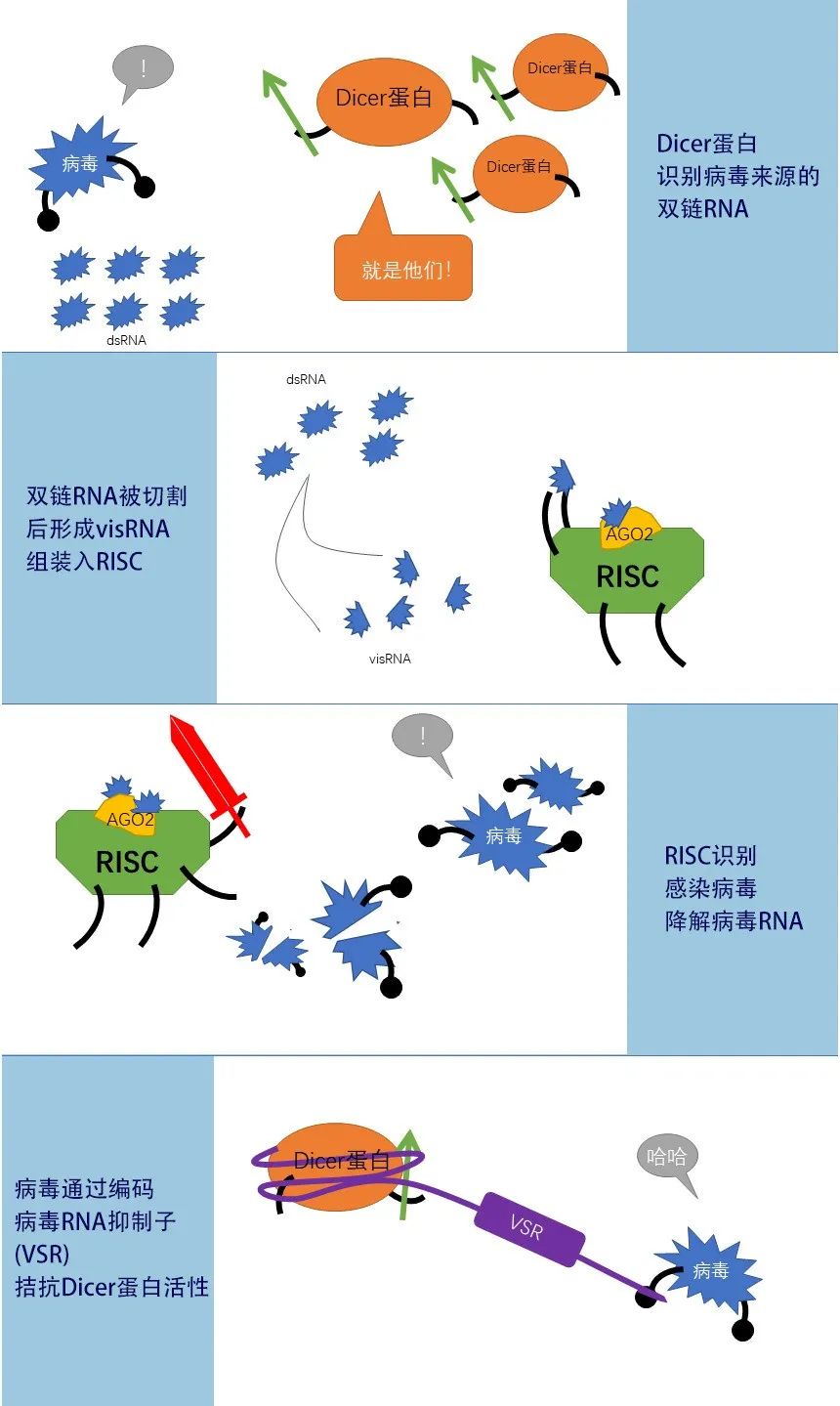
哺乳动物中RNAi免疫机制的发现
VSR靶向多肽:药物研发新方向
在该项研究中,研究团队创新性地根据肠道病毒EV-A713A VSR蛋白的A1和A2螺旋序列人为设计了P1、P2两个VSR靶向肽(VSR-targeting peptide,VTP)。通过检测选取细胞系中EV-A71 RNA的积累状况,表明P1和P2都以剂量依赖的方式有效抑制了病毒的复制。
之后根据实验效果,参照效果较优的P2序列进一步合成了一系列多肽,发现其中肽ER的D-逆转录转化修饰亚型 (ER-DRI) 对病毒RNA复制的抑制效果最好。为证实该系列VTP靶向并灭活EV-A71 3AVSR,解锁RNAi的抗病毒活性,感染细胞中总RNA被提取并进行了深度测序,结果表明被检测到的vsiRNA的确来源于EV-A71。其中,被感染细胞内EV-A71病毒RNA纯化提取使用Qiagen及Foregene病毒总RNA提取试剂盒进行。
同时,对发生突变缺失了3A-VSR功能的EV-A71病毒,以及被EV-A71病毒感染的Dicer1或AGO2缺失细胞,VTP均无法发挥抗病毒作用。证明其作用机制确实是靶向3A-VSR,并依赖于RNAi通路。
为了研究ER-DRI的临床前潜力,研究团队通过腹腔注射荧光标记肽,评估其在EV-A71病毒感染小鼠中的抗病毒效果。结果表明ER-DRI在小鼠体内同样激发了RNAi抗病毒免疫反应,抑制了EV-A71的复制,改善了感染小鼠的临床症状,并减少了感染导致的小鼠死亡。同时急性毒性试验表明,ER-DRI对小鼠的健康不存在明显危害。
VTPs解锁的RNAi免疫机制强大到足以介导高效的抗病毒活性,明确地证明了RNAi作为哺乳动物抗病毒免疫的生理重要性和治疗可行性。此外,该研究已经证明了VSRs是可药物化的靶点,为抗病毒治疗提供了靶向 VSRs的全新策略,并且像ER-DRI这样的多肽作为肠道病毒感染的一流VTD有相当大的前景。
关注福际生物,持续为您带来分子前沿信息